FOXP3(forkhead box P3)またはScurfinは、免疫応答に関与するタンパク質である。FOXP3はFOXタンパク質ファミリーのメンバーであり、制御性T細胞(Treg)の発生と機能の調節経路のマスターレギュレーターとして機能する。一般的に、制御性T細胞は免疫応答を抑える役割を果たす。がんでは制御性T細胞の過剰な活性によってがん細胞が免疫系による破壊を免れている場合があり、また自己免疫疾患では制御性T細胞の活性の欠乏によって他の自己免疫細胞による自組織への攻撃が行われるようになっている場合がある。
その正確な制御機構は十分には解明されていないものの、FOXタンパク質群は類似したDNA結合特性によって転写制御を行っていると考えられている。制御性T細胞のモデル系では、FOXP3は制御性T細胞の機能に関与する遺伝子群のプロモーターに結合し、またT細胞受容体刺激後に重要な遺伝子の転写を阻害している可能性がある。
遺伝子
FOXP3遺伝子は11個のエクソンから構成される。マウスとヒトの遺伝子でコーディング領域のエクソン-イントロン境界は同一である。FOXP3遺伝子はX染色体の短腕(Xp11.23)に位置する。
生理
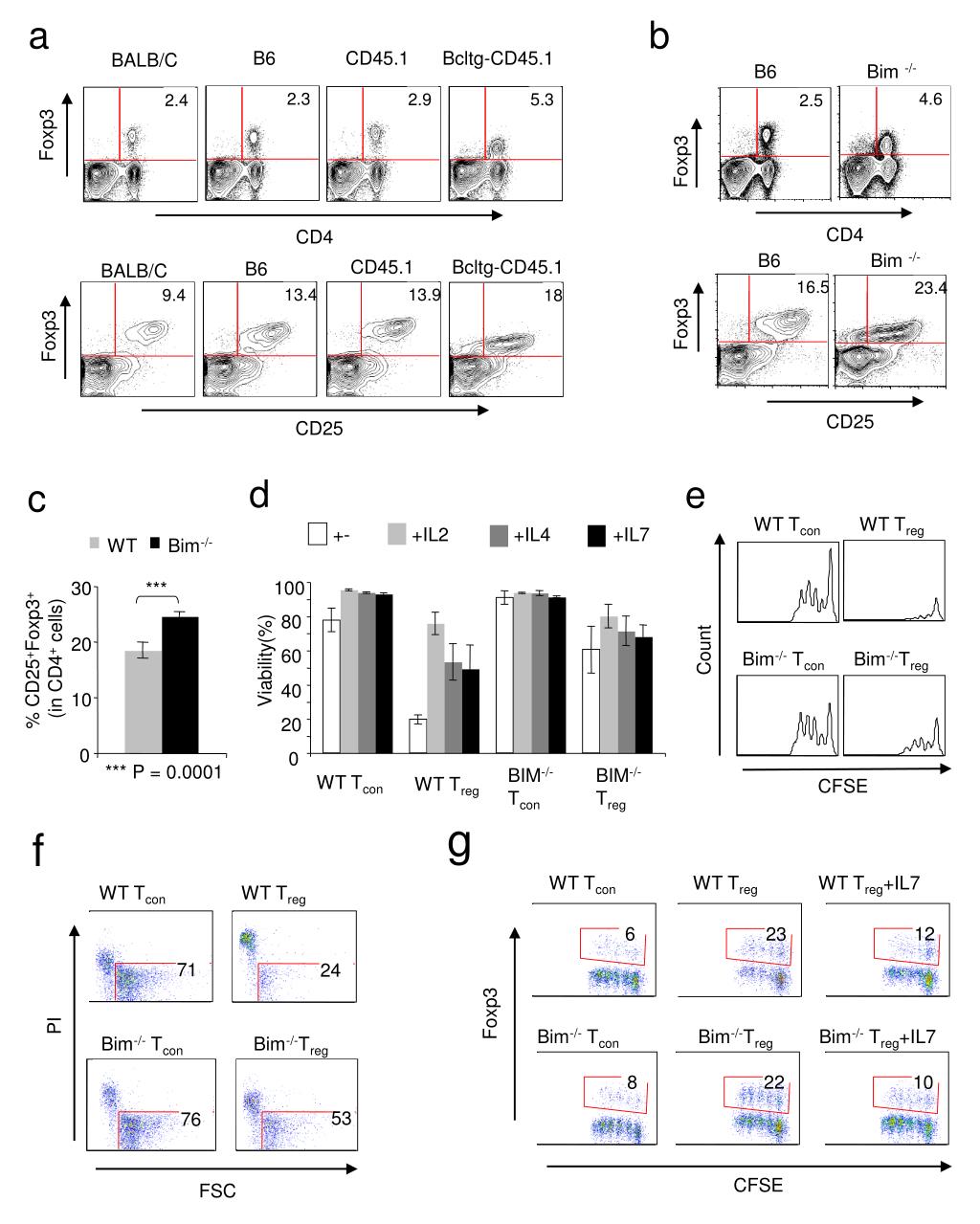
FOXP3は内在性Treg(nTreg)や誘導性Treg(iTregまたはaTreg)の特異的マーカーであり、またこれらの細胞はCD25、CD45RBなどのより特異性の低いマーカーによっても同定される。動物研究では、Foxp3を発現するTregは免疫寛容、特に自己寛容に重要であることが示されている。
動物研究では、糖尿病、多発性硬化症、気管支喘息、炎症性腸疾患、甲状腺炎、腎臓病モデルにおいて、Foxp3陽性T細胞の誘導または投与によって自己免疫疾患の重症度が顕著に低減されることが示されている。ヒトにおいても、Tregを用いた移植片対宿主病の治療の有効性が示されている。
一方、T細胞は当初考えられていたよりも可塑性が高いことが示されている。このことは治療におけるTregの利用がリスクを伴う可能性を意味しており、一例として宿主へ投与されたTregは炎症促進性のTh17細胞へ変化する可能性がある。Th17細胞が産生される環境はiTregと類似しており、Th17細胞はTGF-βとIL-6(またはIL-21)の影響下で産生されるのに対し、iTregはTGF-βのみの影響で産生される。
FOXP3はTreg系列のマスターレギュレーターとして同定されており、ヒストン標識に依存してアクチベーターとしてもリプレッサーとしても機能する。FOXP3遺伝子の発現はナイーブT細胞からTregへの変換をもたらすことが知られており、Tregはin vivoやin vitroで免疫抑制能を有する。このことは、FOXP3が免疫抑制を媒介する因子の発現を調節していることを示唆しており、FOXP3の標的の同定がTregによる免疫抑制の理解に重要となる可能性を示している。
病態生理
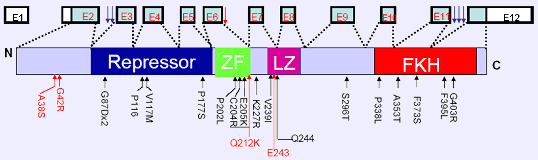
Tregの数の変化、特にFOXP3を発現している細胞の数の変化は、多くの疾患でみられる。一例として、腫瘍を有する患者ではFOXP3陽性T細胞が局所的に相対的に過剰に存在し、がん細胞形成を抑制する能力が阻害されている。逆に、全身性エリテマトーデスなどの自己免疫疾患の患者では、FOXP3陽性細胞が相対的に機能不全を起こしている。また、IPEX症候群ではFOXP3遺伝子に変異が生じている。IPEX症候群の患者の多くでは、DNA結合を担うフォークヘッドドメイン領域に変異が生じている。
マウスでは、Foxp3の変異(フォークヘッドドメインの喪失が引き起こされるフレームシフト変異)によって"Scurfy"と呼ばれるX連鎖劣性遺伝変異体マウスとなり、ヘミ接合型オスマウスは出生後16から25日で致死となる。この変異体マウスでは、CD4 T細胞の過剰増殖、広範囲にわたる多臓器浸潤、多数のサイトカインの上昇が生じる。この表現型は、CTLA-4やTGF-βの発現を欠くマウスや、IPEX症候群のものとも類似している。Foxp3遺伝子を過剰発現するマウスでは、T細胞数の減少が観察される。残りのT細胞も増殖能や細胞溶解応答、IL-2産生が乏しいが、胸腺の発生は見かけ上正常である。組織学的解析では、末梢リンパ器官、特にリンパ節で正常な細胞数がみられない。
がんにおける役割
FOXP3の多型(rs3761548)は、Tregの活性や、IL-10、IL-35、TGF-βといった免疫調節サイトカインの分泌に影響を及ぼすことで、胃がんなどの発生に寄与している可能性がある。P60と呼ばれる15-merの合成ペプチドは細胞内へ移行してFOXP3に結合し、FOXP3の核移行を妨げることが示されている。その結果、FOXP3はNF-κBやNFATといった転写因子を抑制することができなくなる。こうしたFOXP3阻害ペプチドによってTregの機能を阻害することで、抗腫瘍免疫療法の効果を高めることができる可能性がある。
自己免疫
FOXP3調節経路の変異や破綻は、自己免疫性甲状腺炎や1型糖尿病といった器官特異的自己免疫疾患につながる場合がある。こうした変異は胸腺内で発生する胸腺細胞に影響を及ぼす。胸腺細胞はその分化の際に、FOXP3によって調節を受けて成熟型Tregへ形質転換する。全身性エリテマトーデスの患者の一部にはこの過程に影響を及ぼすFOXP3変異がみられるが明らかにされており、胸腺内で適切なTreg細胞の発生が生じなくなっている。こうした機能不全型Treg細胞は転写因子による効果的な調節を受けず、健康な細胞を攻撃することで器官特異的な自己免疫疾患につながる。また、FOXP3は炎症抑制を媒介する分子の発現調節を介して、自己免疫系の恒常性を維持ししている。一例として、FOXP3はCD39の発現を誘導し、細胞外のATPの分解促進をもたらす。CD39は炎症性分子であるATPを抗炎症分子であるアデノシンへ分解するカスケードの律速段階となる酵素であり、さまざまな細胞集団で免疫抑制を調節する。
出典
関連文献
関連項目
- AIRE
- 免疫
- 自己免疫
- 中枢性免疫寛容
- IPEX症候群
- リンパ球
- 胸腺細胞
外部リンク
- GeneReviews/NIH/NCBI/UW entry on IPEX Syndrome
- FOXP3 protein, human - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス(英語)